固相多肽合成法(SPPS)几乎彻底改变了所有多肽原料药的生产方式。SPPS最初由布鲁斯·梅里菲尔德开发出来,主要采用一种惰性固相合成树脂,将C-末端氨基酸固定在肽链中,从而消除其在连续的链延伸周期中的反应性。因此,通过在侧链功能上运用氨基保护基和半永久型保护基团,一个肽分子可以以矢量的方式,从C端到N端进行组装。过去40年,不论是在运用Boc-Bzl法还是Fmoc-tBu法上都在不断地演变。前者主要使用强酸如三氟乙酸(TFA)裂解Boc保护基,后者用碱去除Fmoc保护基。Fmoc策略最终成为了最受欢迎的方法,因为其消除了使用HF体系切割的繁琐和危险性。HF体系在切割和脱保护肽时需使用Boc-Bzl策略,并且有必要加上特别的聚三氟氯乙烯和聚四氟乙烯设备,就为了能安全地使用HF切割液。Fmoc-tBu法合成多肽的典型酸解切割可以在标准化玻璃反应釜内进行,并易于扩展的。
与SPPS相比,液相法就显得尤为慢速。液相化学的经济效益在于减少化学废弃物的产生,以及因反应均一性只用于非常小的摩尔过量的情况下,产生更少量的关键氨基酸衍生物。此外,通常使用带有不稳定氢保护基(Z基)的特殊保护氨基酸衍生物。同时,氢化去除这些保护基对商业化生产也造成了相当大的危害。通常,C-末端氨基酸作为不稳定酯酸受到保护。在耦合反应之后,有必要采取一系列的有机萃取和水萃取去除试剂和多余的反应物,即在进行下一步之前,移出Z保护基。这就造成了一个缓慢并且繁琐的工艺,只有在非常大的商业规模下才实用。
因此,一个理想的解决方案是开发特殊的化学方法,使得液相反应与固相十分相似。如果真的有这个可能,那么在简单的液相方法中使用Fmoc-tBu氨基酸衍生物也许是可行的。该方法的益处主要在于随时可用的标准Fmoc-tBu氨基酸衍生物的经济化利用,以极其合理的成本,降低液相工艺过程废弃物的产生。现在出现了两种类似的技术可以使这一点变得实用。而这两种技术都依赖一种特殊的C-末端保护基团,在消除该位置的反应性的同时,赋予保护肽独特的溶解度特性,这样有助于保持其有机溶剂型偶联和脱保护步骤在溶液中的能力,但与水洗溶液相比,更加便于提取或沉淀。
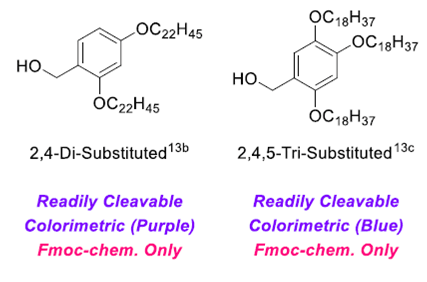
由日本Jitsubo株式会社研发的工艺是用一个C-末端酯化保护基团,该保护基团具有一个中心苯甲醇的一部分和两个长烷基侧链,使其在乙腈中不溶(如上图所示)。他们将其工艺命名为Molecular Hiving(一种疏水标签标记辅助的液相多肽合成技术)。液相化学工艺步骤在一些特别的绿色溶剂中得到了发展,例如2 Me-THF(2-甲基四氢呋喃)替代了DMF(N,N-二甲基甲酰胺)和NMP(N-甲基吡咯烷酮)。在反应结束时,产物将沉淀到MeCN(乙腈)中,然后该沉淀物用MeCN洗涤,以去除试剂和反应物,以及用丙胺去除未反应的氨基酸。沉淀产物随后在Me-THF中重新分解,然后继续下一个循环。
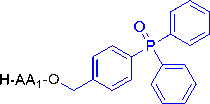
第二种类似的技术是采用一种C端酯化链接剂与二苯基膦苯甲醇相结合,被命名为GAP试剂(基团辅助纯化),如下图所示。这项技术是由美国的GAP Peptides公司研发的。技术的延伸是将Fmoc-tBu固相多肽合成法(SPPS)常用的标准链接剂加入GAP试剂中,从而更容易获得肽酸和酰胺。该化学方法能使均相液相工艺通过沉淀/萃取步骤去除试剂和反应物。该工艺还能便于Fmoc-tBu方法应用于液相工艺,使传统的反应釜将各阶段分离实现工艺自动化,并使有机层保留99%以上的生长肽。
参考文献
(1) Merrifield, R.B.(1963年)《美国化学学会杂志》 85 (14): 2149–2154
(2) Okada. Y. et al.(2019年)《有机工艺研究与开发》 23, 2576−2581
(3) Siefert, C.W. et al.,(2016年)《欧洲有机化学》 10.1002/ejoc.201600026

 英语
英语